Biotecnología
Embriones sintéticos de ratón desarrollan cerebros y corazones en forma autónoma
Nueva y revolucionaria vía para recrear en laboratorio las primeras etapas de la vida embrionaria
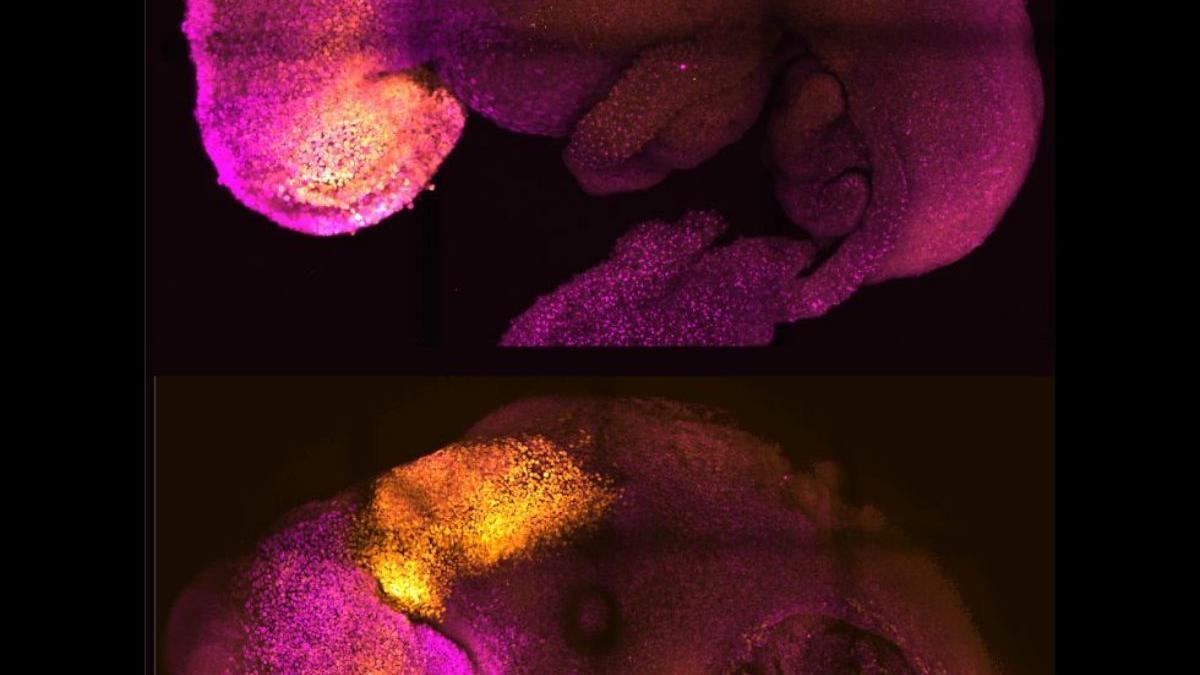
Embriones naturales (arriba) y sintéticos (abajo) demuestran una formación cerebral y cardíaca comparable. / Crédito: Amadei and Handford.
Pablo Javier Piacente
Embriones de ratón gestados en laboratorio desarrollaron cerebros y corazones palpitantes, como si fueran reales. Los embriones sobrevivieron durante 8,5 días: los científicos modificaron genéticamente a las células madre de ratón para que se convirtieran en embriones sintéticos, que comenzaron a desarrollar corazones y cerebros. El avance podría dar pistas sobre cómo se concretan las primeras etapas del desarrollo embrionario en los humanos.
Un grupo de investigadores de la Universidad de Cambridge, en Reino Unido, ha creado embriones modelo a partir de células madre de ratón que forman un cerebro, un corazón que late y los cimientos de todos los demás órganos del cuerpo. Se trata de una nueva y revolucionaria vía para recrear las primeras etapas de la vida.
Según un
nota de prensa
, el equipo de especialistas dirigido por la profesora Magdalena Zernicka-Goetz creó un modelo de embrión sin óvulos ni espermatozoides. En su lugar, el desarrollo se concreta mediante células madre, que son las células maestras del cuerpo, capaces de convertirse en casi cualquier tipo de célula de un organismo.
Interacción entre células madre
Al imitar los procesos naturales que guían a los tres tipos de células madre que se encuentran en el desarrollo temprano de los mamíferos hasta comenzar su interacción y propiciar el desarrollo de nuevas células, los científicos pudieron conseguir que las células madre se comunicaran entre sí y concretaran ese proceso de forma sintética. El nuevo estudio fue publicado recientemente en la revista Nature.
Las células madre se organizaron en forma independiente en estructuras que progresaron a través de las sucesivas etapas de desarrollo hasta que tuvieron corazones latiendo y los cimientos del cerebro, así como el saco vitelino en el cual el embrión se desarrolla y obtiene nutrientes en sus primeras semanas.
A diferencia de otros embriones sintéticos, los modelos desarrollados por los investigadores británicos llegaron al punto en que todo el cerebro, incluida la parte anterior, comenzó a desarrollarse. Los embriones sintéticos lograron sobrevivir durante un período de 8 días y medio.
Un avance trascendente
El nuevo trabajo produjo resultados muy similares a los conseguidos por una
investigación anterior
, publicada el 1 de agosto en la revista Cell. Sin embargo, en este caso el grupo de investigación conducido por Zernicka-Goetz comenzó con tres tipos de células madre de ratón, en lugar de comenzar solo con células “ingenuas” como los científicos de la investigación previa. Una célula “ingenua” o
célula T naive
es un tipo de célula madre que da origen al embrión: las otras tipologías se transforman en los tejidos de la placenta y el saco vitelino.
Este enfoque diferente les permitió observar cómo interactuaban estos tres tipos de células madre, intercambiando mensajes químicos y colisionando físicamente entre sí en el experimento. En el análisis de estos intercambios se pueden obtener pistas sobre cómo se ponen en marcha las primeras etapas del desarrollo embrionario en los humanos, y qué sucede cuando ocurre algún problema en ese proceso.
Estos estudios han suscitado diferentes reacciones en la comunidad científica internacional. Según
declaraciones
para Science Media Centre España, el profesor e investigador de la Universidad Pompeu Fabra, Alfonso Martínez Arias, indicó que “este último trabajo es una adición importante al publicado por el grupo de Jacob Hanna en Cell hace unos días. Los dos representan un avance importante, pues prueban la necesidad de interacción entre células embrionarias y extraembrionarias en la formación de un mamífero. Más aún, demuestran que es posible iniciar el desarrollo de un mamífero fuera del útero”, concluyó el especialista.
Referencia
Synthetic embryos complete gastrulation to neurulation and organogenesis
. Gianluca Amadei, Magdalena Zernicka-Goetz et al. Nature (2022). DOI:
https://doi.org/10.1038/s41586-022-05246-3
- #PapaGorda24: las borracheras más vergonzosas de la Feria de Abril
- Deco solo planea dos fichajes para el Barça
- El Barça rechaza una oferta de 60 millones por Raphinha
- El Mono Burgos justifica su comentario sobre Lamine Yamal
- Roberto Brasero alerta de la llegada de 'Sancho': la borrasca que pone en riesgo a varias zonas de España
- El Barça vestirá Nike, al menos, hasta el 2028
- Barcelona - PSG, en directo hoy: alineaciones, horario y dónde ver el partido de Champions League
- La maldita cláusula de Haaland asusta al Barça